Sådan finder du massefylden af vand
Forfatter:
Roger Morrison
Oprettelsesdato:
21 September 2021
Opdateringsdato:
1 Juli 2024

Indhold
I denne artikel: Find tætheden af vandForstå begrebet tæthed5 Referencer
Tæthed er massen af et objekt pr. Volumenhed (det rum, som objektet besætter). Densitetsenheden er gram pr. Ml (g / ml). At finde massefylden af vand er relativt enkelt og gøres takket være formlen densitet = masse / volumen.
etaper
Del 1 Finde vandets densitet
-

Saml de nødvendige materialer. For at beregne vandtætheden har du brug for en gradueret cylinder, en skala og vand. Graderede cylindre er specielle containere med linjer eller graderinger, der giver dig mulighed for at måle en bestemt mængde væske. -

Vej den graderede cylinder tom. For at finde massefylden, skal du først kende massen og volumen på den pågældende væske. Du bruger den graduerede cylinder til at få massen af vand, men du bliver nødt til at trække massen af den graduerede cylinder fra den samlede masse.- Tænd for skalaen, og kontroller, at den er indstillet til nul.
- Placer den tørre, tomme graderede cylinder på skalaen.
- Registrer cylindermassen i gram (g).
- Forestil dig for eksempel, at den tomme graderede cylinder vejer 11 gram.
-
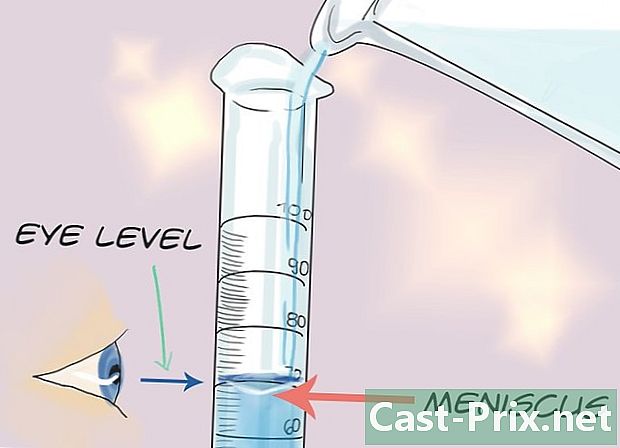
Fyld den graduerede cylinder med vand. Mængden af vand betyder ikke noget. Det er meget vigtigt at bemærke denne mængde. Læs lydstyrken ved at placere blikket godt foran vandstanden og noter værdien i bunden af menisken. Menisken er den buede del af væskeoverfladen, som du ser, når vandstanden er lige foran dine øjne.- Vandmængden af den graduerede cylinder er den, du vil bruge til beregning af densitet.
- Forestil dig, at du fyldte den graduerede cylinder med 7,3 ml vand.
-

Vej den graduerede cylinder fyldt med vand. Kontroller, at skalaen viser nul, og vej cylinderen fyldt med vand. Pas på ikke at spildes under drift.- Hvis du spilder vand, skal du notere den nye mængde vand i ml og veje den vandfyldte cylinder igen.
- Forestil dig for eksempel, at den graduerede cylinder nu vejer 18,3 gram.
-

Træk massen af den tomme cylinder fra massen af den fulde cylinder. For at få massen af vand skal du trække massen fra den graduerede cylinder. Resultatet repræsenterer massen af vand til stede i den graduerede cylinder.- I vores eksempel er massen af den graduerede cylinder 11 g, mens cylindrens masse er 18,3 g. 18,3 g - 11 g = 7,3 g. Vand vejer 7,3 gram.
-

Beregn densiteten. Derefter skal du dele massen med lydstyrken. For at bestemme vandets densitet skal du bruge følgende ligning: densitet = masse / volumen. Indtast den masse og volumen, du har bestemt i ligningen, og find værdien på densiteten.- Masse vand: 7,3 g
- Vandmængde: 7,3 ml
- Vandtæthed = 7,3 / 7,3 = 1 g / ml
Del 2 Forståelse af begrebet tæthed
-

Definer densitetsligningen. Densiteten er lig med massen m et objekt divideret med lydstyrken v af det samme objekt. Densiteten er repræsenteret ved det græske bogstav rho: ρ. Et tættere objekt vil have en større masse for et mindre volumen sammenlignet med et objekt med lavere densitet.- Standard ligning af densitet er som følger: ρ = m / v.
-
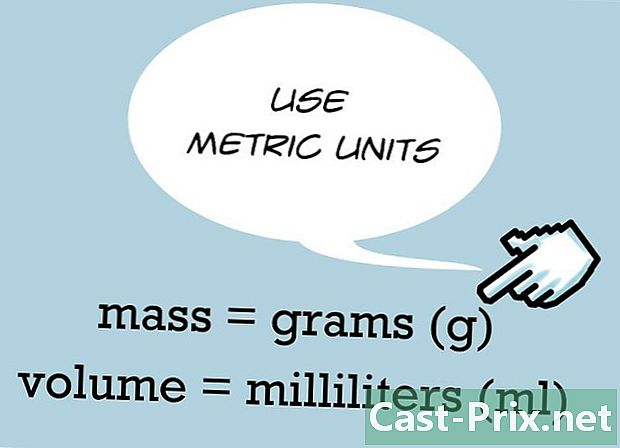
Brug de relevante enheder til hver variabel. Ved beregning af en densitet er det sædvanligt at angive måleenheder. Massen af et objekt er angivet i gram, mens volumenet er angivet i milliliter. Du kan også se mængder i kvadratcentimeter (cm). -

Ved, hvordan densitet er et vigtigt koncept. Et objekts tæthed kan bruges til at identificere forskellige materialer. Hvis du prøver at identificere et stof, kan du beregne dens densitet og sammenligne det med kendte massefyldematerialer. -

Forstå, hvilke faktorer der kan påvirke vandtætheden. Selvom dette generelt er tæt på 1 g / ml, er det nødvendigt at opnå større præcision for visse videnskabelige discipliner. Densiteten af rent vand ændres efter temperatur. Det steg, når temperaturen faldt.- For eksempel ved 0 ° C er vandets densitet 0,9998 g / ml, men ved 80 ° C er den 0,9818 g / ml. Disse forskelle kan virke små, men de er vigtige at kende til forskning og videnskabelige eksperimenter.

